西南大学发现胶质母细胞瘤诊疗新靶点
发布时间:2023-09-16 22:50:07
胶质母细胞瘤是人类最常见、最具侵袭性的原发性中枢神经系统肿瘤。尽管在神经成像、神经外科技术、放疗和化疗方面等取得了一定的进展,但在过去几十年里,胶质母细胞瘤患者的总体生存率仍未有效改观。因此,如何对胶质母细胞瘤进行早期诊断、靶向干预和预后评估,进而提高患者生存率是亟待解决的临床问题。
PARP1抑制剂是一种靶向聚ADP核糖聚合酶的癌症疗法。它是第一种成功利用合成致死概念获得批准在临床使用的抗癌药物。然而,对PARP1抑制剂最初有应答的大多数患者可能逐渐发展为 PARP抑制剂耐药;而那些在病程后期接受 PAPR 抑制剂治疗的患者,随着既往治疗线的增加,客观缓解率逐步下降。 PARP1被证实还参与了多种细胞过程,如 DNA的复制、重组、转录、细胞增殖和凋亡等。因此,深入探究PARP1参与的其他信号途径,优化基于PARP1分子治疗机制的联合治疗,实现药物的协同作用是分子靶向治疗的最终目标。
医学研究院崔红娟教授团队在神经系统肿瘤领域的权威期刊Neuro-oncology(中科院一区TOP期刊, IF=15.9)在线发表文章“NCAPG promotes the progression of glioblastoma by facilitating PARP1-mediated E2F1 transactivation”。研究证实了NCAPG可作为胶质母细胞瘤的关键致癌因子,并可为聚(ADP-核糖)聚合酶PARP1扩增的胶质母细胞瘤患者提供新的潜在治疗靶点。
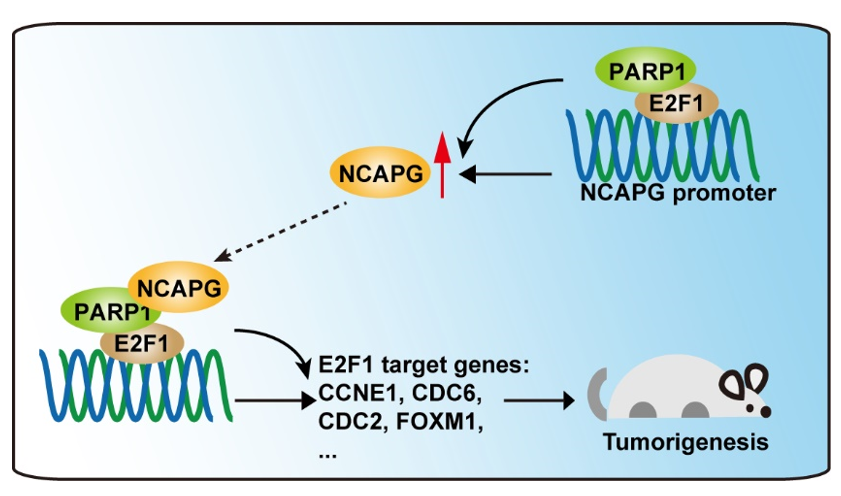
PARP1作为E2F1的转录共激活因子通过调控E2F1信号通路促进肿瘤恶性进展。本研究发现NCAPG (非SMC凝聚素I复合亚基G) 可通过与PARP1直接结合,增强PARP1-E2F1的相互作用,正向调节E2F1信号通路活性。此外,通过ChIP和双荧光素酶实验,发现E2F1可转录调控NCAPG的表达。综合数据挖掘和免疫组化实验分析表明,NCAPG的表达与PARP1/E2F1信号轴呈正相关,是胶质母细胞瘤患者预后不良的重要指标。上述研究结果揭示了一种新机制, E2F1转录激活NCAPG的表达,进而增强PARP1和E2F1之间的相互作用,持续增强E2F1的反式活化。这些发现表明NCAPG/PARP1/E2F1轴在GBM进展中的关键作用,为基于PARP1抑制剂的联合治疗提供了潜在的靶点。
综上,此项研究从临床问题出发,通过多组学技术挖掘潜在的PARP1分子治疗靶点,并通过细胞与动物模型验证其作用与机制,为胶质母细胞瘤的诊断与干预技术的研发奠定了重要基础。
西南大学为第一单位,青年教师侯建兵为论文第一作者,崔红娟教授为论文通讯作者。此项研究获得了重庆市自然科学基金及中央高校基本科研基金项目的支持。